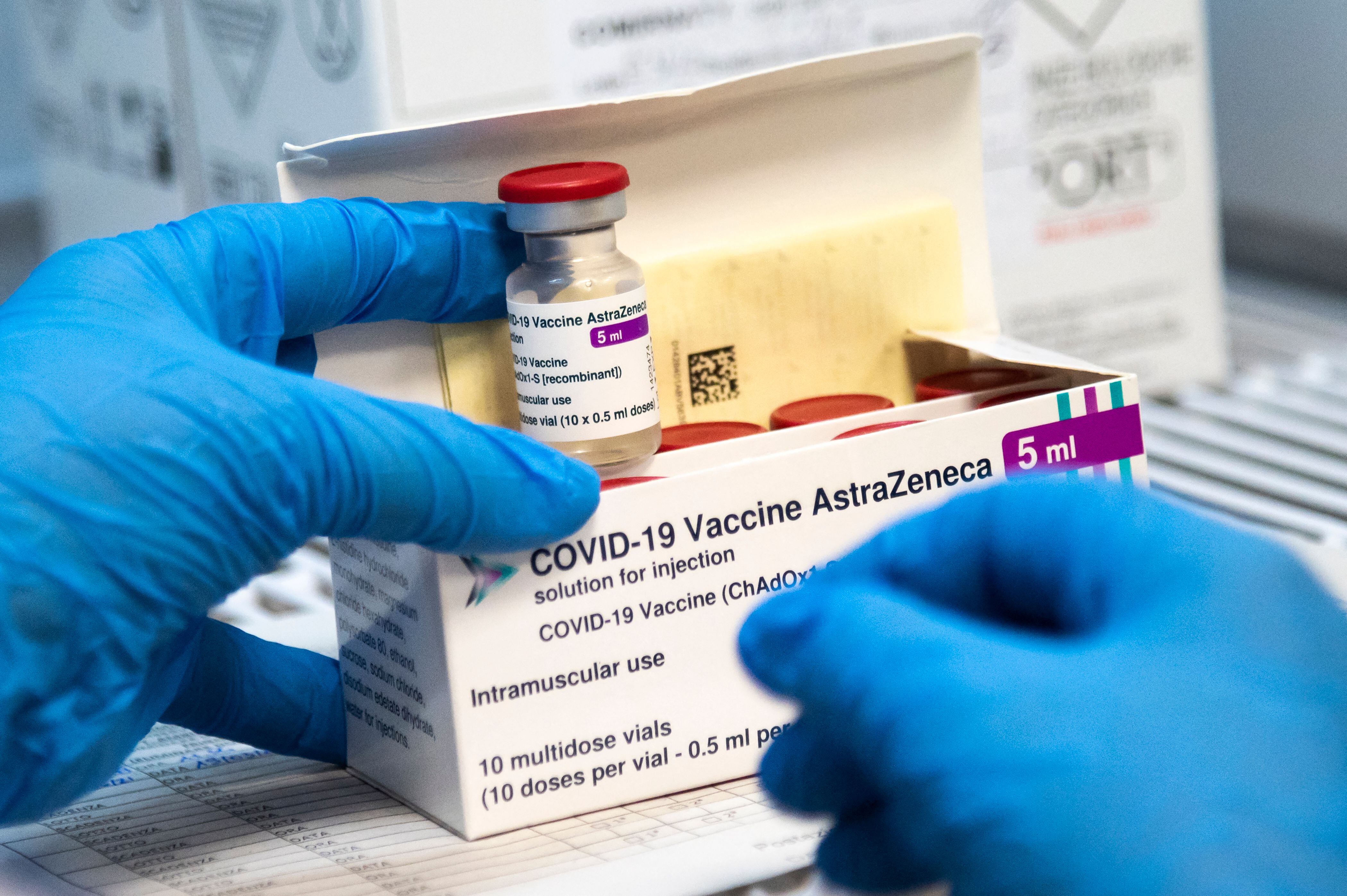
¿Cómo explicar los graves ―e inusuales― problemas sanguíneos observados en algunas personas vacunadas contra la COVID-19 con AstraZeneca? Esta cuestión acuciante todavía carece de respuesta, a unos días de la reunión de la Agencia Europea de Medicamentos (EMA) de la semana próxima.
¿Qué se ha observado?
Los problemas observados en algunas personas vacunadas con AstraZeneca no son trombos corrientes (formación de coágulos sanguíneos), como se informó en un principio, sino un fenómeno “muy atípico”, subrayó la Agencia Francesa de Medicamentos (ANSM).
Se trata de “trombosis de las venas grandes, atípicas por su localización (cerebral en su mayoría, pero también digestiva), que pueden estar asociadas a una trombocitopenia (un déficit de plaquetas sanguíneas) o a problemas de coagulación”, como hemorragias, según la ANSM.
A mediados de marzo, el instituto médico Paul-Ehrlich (PEI), que asesora al gobierno alemán, dio cuenta de una "acumulación sorprendente de una forma específica de trombosis venosa cerebral muy inhabitual, asociada a un déficit de plaquetas sanguíneas".
LEA MÁS: AstraZeneca enfrenta crisis política y de imagen
Según los especialistas, este cuadro muy específico conduce a pensar en un fenómeno llamado coagulación intravascular diseminada (CIVD).
Se trata de “síndromes excepcionales, que se dan en casos de septicemias graves” y que pueden traducirse en “trombosis y hemorragias”, explicó recientemente a la AFP la infectóloga Odile Launay, miembro del Comité de vacunas anticovid creado por el gobierno francés.
¿Qué relación guarda con la vacuna?
“No se ha probado ninguna relación de causalidad, pero es posible y se están realizando análisis suplementarios”, dijo el miércoles la Agencia Europea de Medicamentos (EMA), que volverá a reunirse para tratar de este tema del 6 al 9 de abril.
Sin embargo, otros especialistas de Europa fueron más categóricos.
"Hay que dejar de especular para saber si existe una relación o no. Todos esos casos tuvieron síntomas entre tres y diez días después de la inyección de AstraZeneca. No hemos encontrado ningún otro factor detonante", explicó el 27 de marzo a la cadena noruega TV2 Pål André Holme, jefe de un equipo del Hospital Nacional de Oslo, que trabaja en esos casos.
"La agencia noruega de medicamentos considera que existe una relación probable con la vacuna", declaró a la AFP Steinar Madsen, uno de sus responsables.
Por su parte, la ANSM confirmó el 26 de marzo la existencia de un riesgo "escaso", basándose en "el carácter muy atípico de esas trombosis, sus cuadros clínicos próximos y el plazo de aparición, homogéneo".
¿Cuál es el riesgo?
Esa es la principal cuestión.
Según cifras de la EMA, presentadas el miércoles, se han detectado hasta la fecha 62 casos de trombosis venosas cerebrales en el mundo, incluyendo 44 en los 30 países del Espacio Económico Europeo (UE, Islandia, Noruega, Liechtenstein), por 9,2 millones de dosis de vacuna administradas.
Se han registrado 14 decesos, aunque no se han podido atribuir de manera segura a esas trombosis atípicas, precisó la directora de la EMA, Emer Cooke, el miércoles en una videoconferencia.
No obstante, la agencia precisó que esos datos eran fragmentados.
En Alemania, se han reportado 31 casos sospechosos de trombosis venosa cerebral (19 de los cuales estaban acompañados de un descenso de las plaquetas sanguíneas), con 9 decesos, según el Instituto Paul-Ehrlich. Eso representa 1 caso por cada 100.000 dosis de vacuna AstraZeneca administradas (2,8 millones).
También se registraron casos en Francia (12 casos, incluyendo 4 decesos, por 1,9 millones de inyecciones, según la ANSM); en Noruega (5 casos, incluyendo 3 fallecimientos, por 120.000 inyecciones) y en Holanda.
El Reino Unido, que empleó en gran medida ese inmunizante en su campaña de vacunación, en el balance emitido el sábado menciona 30 casos, entre ellos siete muertes, de un total de 18,1 millones de dosis administradas.
Pero, como sucede con todos los medicamentos, la clave está en ponderar los riesgos y los beneficios.
"Los beneficios de la vacuna AstraZeneca en la prevención del covid-19, que comporta hospitalizaciones y muertes, pesan más que los riesgos de efectos secundarios", insistió la EMA el miércoles, como había hecho el 18 de marzo tras las primeras alertas.
¿Factores de riesgo?
De momento, la mayoría de casos sucedieron en personas menores de 65 años, mujeres en su mayoría. Pero no se pueden extraer conclusiones, pues esto puede deberse a que esa vacuna se ha utilizado inicialmente, sobre todo, en jóvenes.
Además, el hecho de que sobre todo haya mujeres en los casos registrados puede deberse a que la vacuna se ha usado mucho en la vacunación del personal sanitario, una categoría prioritaria de población. Un sector en el que trabajan muchas mujeres.
"De momento, los exámenes no identificaron factores de riesgo específicos para esos hechos muy aislados, como la edad, el sexo o un historial médico que incluya problemas de coágulos sanguíneos", indicó la EMA.
Aún así, después de la primera oleada de suspensiones, a mediados de marzo, algunos países decidieron dejar de utilizar la vacuna por debajo de una determinada edad.
El martes, Alemania decidió restringir su uso a los menores de 60 años y Canadá suspendió su utilización en menores de 55 años. Francia dejó de usarla en menores de 55 años y Suecia y Finlandia, de 65 años.
"No solo tenemos una vacuna, tenemos varias. Por eso, me parece que tiene sentido reservar la de AstraZeneca para las personas mayores", declaró una viróloga de la Universidad Goethe de Fráncfort, Sandra Ciesek, a la revista Science.
Noruega y Dinamarca optaron por suspender totalmente el uso de la vacuna, de momento.
¿A qué se debería?
De momento, se han formulado varias hipótesis, que la EMA tendrá que aclarar.
En un estudio publicado en línea el 28 de marzo, pero que todavía no fue evaluado por otros científicos, investigadores alemanes y austriacos establecieron un símil con otro mecanismo ya conocido.
El fenómeno asociado a la vacuna de AstraZeneca "se parece clínicamente a la trombocitopenia inducida por heparina (TIH)", indicó el equipo de científicos, liderado por Andreas Greinacher (Universidad de Greifswald).
La TIH es una reacción inmunitaria anormal, grave e inhabitual desencadenada en algunos pacientes por un medicamento anticoagulante, la heparina.
El grupo de investigadores propone que se le dé un nombre al fenómeno observado con la vacuna de AstraZeneca (el acrónimo en inglés VIPIT).
El 18 de marzo, el equipo del Hospital Nacional de Oslo ya había considerado que esos casos podían explicarse por "una potente respuesta inmunitaria" provocada por la vacuna.
El colectivo de investigadores y médicos francés "Du côté de la science" (Del lado de la ciencia) también apuesta por "una reacción inmunitaria intensa" y plantea la hipótesis de que todo empiece con "la inyección accidental de la vacuna en una vena del músculo deltoides" (en el hombro).
“En presencia de factores no identificados integralmente”, esta “inyección intravenosa accidental [...] provocaría una reacción inmunitaria discordante”, apunta el colectivo de científicos en su página web.
Vector viral
Esta vacuna fue desarrollada por los investigadores de la universidad de Oxford en colaboración con gigante farmacéutico británico AstraZeneca.
Es una vacuna “de vector viral”: toma como base otro virus (un adenovirus de chimpancé) que fue debilitado y genéticamente modificado para impedir que el coronavirus se reproduzca en el organismo humano.
La forma en que introduce el material genético en las células, ordenándoles que ataquen al SARS-CoV-2, se ha calificado de “caballo de Troya”.
Práctica y asequible
La vacuna de AstraZeneca/Oxford tiene la ventaja de ser barata (unos 2,5 euros o $3 por dosis, con variaciones según los costes de producción locales). AstraZeneca se ha comprometido a venderla sin hacer beneficio.
También es fácil de almacenar: puede conservarse a la temperatura de un refrigerador, entre 2ºC y 8ºC, a diferencia de las vacunas de Moderna y Pfizer/BioNTech, que solo pueden almacenarse a largo plazo a temperaturas muy bajas.
Esto facilita una vacunación a gran escala.
Este fármaco, además, es distribuido mediante el programa Covax a los países más desfavorecidos.
Confusión sobre su eficacia
Según el laboratorio británico, tiene una eficacia promedio del 70% (frente a más de 90% para Pfizer/BioNTech y Moderna), resultado validado por la revista científica The Lancet.
En los primeros resultados publicados, procedentes de ensayos clínicos previos a su aprobación, aparecían variaciones de eficacia, según dosis diferentes administradas por error, lo que sembró la duda y provocó críticas, llevando a la empresa a realizar estudios adicionales.
Su eficacia en personas mayores de 65 años también fue cuestionada en Europa por falta de datos, hasta que nueva información, extraída de las campañas de vacunación de los países más avanzados en este terreno, aportó tranquilidad al respecto.
En Estados Unidos, el regulador de medicamentos criticó al grupo farmacéutico por haber suministrado datos “obsoletos” en sus ensayos clínicos. Por ello, redujo su eficacia a 76% en los casos sintomáticos, en lugar de un 79%.
Dos estudios británicos realizados en condiciones reales, en Escocia e Inglaterra, mostraron una protección importante frente a las hospitalizaciones.
Retrasos en las entregas
Según AstraZeneca, a mediados de marzo, la vacuna estaba aprobada en más de 70 países. El Reino Unido fue el primero en autorizarla y encargó 100 millones de dosis.
Los retrasos en las remesas a los países de la Unión Europea provocaron arduas quejas, ya que el laboratorio sí entregaba al Reino Unido las existencias prometidas. Ante esta falta de suministros, la Comisión Europea decidió controlar las exportaciones de vacunas anticovid para impedir entregas a otros países.
Esta situación causó tensiones entre Bruselas y Londres, pero desde entonces se comprometieron a solucionar el litigio mediante negociaciones.